Ósmosis
La ós
 La palabra ómosis deriva del griego osmos, que significa “empuje” o “impulso”. En 1784 el fenómeno de ósmosis lo descubrió el físico francés Jean Antoine Nollet al experimentar con disoluciones de sacarosa, agua pura y papel pergamino como membrana. No fue sino hasta 1854 que el químico inglés Thomas Graham introdujo el término Ósmosis. La ósmosis del agua es un fenómeno biológico importante para el metabolismo celular de los seres vivos.
La palabra ómosis deriva del griego osmos, que significa “empuje” o “impulso”. En 1784 el fenómeno de ósmosis lo descubrió el físico francés Jean Antoine Nollet al experimentar con disoluciones de sacarosa, agua pura y papel pergamino como membrana. No fue sino hasta 1854 que el químico inglés Thomas Graham introdujo el término Ósmosis. La ósmosis del agua es un fenómeno biológico importante para el metabolismo celular de los seres vivos.
Se denomina membrana semipermeable a la que contiene poros o agujeros, al igual que cualquier filtro, de tamaño molecular. Esta membrana solo permite el paso de algunas moléculas o iones a través de ella.
El incremento del nivel de la disolución con mayor concentración ejerce una presión que se opone a la difusión de las moléculas del agua pura o del disolvente. A esta presión se le conoce como presión osmótica y es la responsable de que las frutas y verduras, las raíces de las plantas y los árboles, así como las células de los organismos animales absorban agua y otros disolventes. El agua pura tiene un valor de presión osmótica 0.
Ósmosis inversa
Aplicaciones
§ Reducción de la dureza: Las aguas duras contienen iones de calcio y magnesio que pueden precipitar combinados con iones como carbonatos, sulfatos o hidróxidos.
§ Descontaminación y tratamiento de efluentes: Para la eliminación de contaminantes en disolución principalmente encaminado al ahorro de agua.
§ Reducción del contenido de nitratos: Con las membranas de ósmosis inversa con un alto porcentaje de rechazo del ion nitrito permite obtener agua con un bajo contenido en dichos iones.
§ Eliminación del color y de los precursores de trihalometanos.
§ Vinazas: El permeado de la ósmosis inversa, que constituye el 90% del volumen inicial de las vinazas, se envía hacia una columna de destilación que permite recuperar el alcohol y otros productos nobles.
§ Alpechines: La ósmosis inversa, combinada con una ultrafiltración, permite recuperar de los efluentes materiales de alto valor económico y obtener agua reutilizable.
§ Usos industriales
o Producción de aguas de alta calidad
o Producción de agua desmineralizada.
o Producción de agua ultrapura.
o Circuitos de refrigeración semiabiertos
o Pintado por electrodeposición: En este proceso la carrocería se sumerge en una dispersión coloidal en agua de partícula de pintura eléctricamente cargada. Tintado de fibras textiles
o Fabricación de catalizadores
o Procesado de papel fotográfico
§ Usos alimentarios
o Fabricación de fécula de patata
o Concentrado de zumos de frutas
o Preconcentración de jugos azucarados
o Preconcentrado de suero lácteo
o Preconcentrado de la clara de huevo
o Estabilización de vinos
o Fabricación de cerveza con bajo contenido en alcohol
o Fermentación alcohólica: La ósmosis inversa puede utilizarse para producir alcohol a partir de los jugos azucarados.
Diálisis

Existen membranas que son permeables no solo a las moléculas del disolvente, sino también a otras moléculas e iones pequeños y que no lo son partículas coloidales. A estas membranas se les llama dializantes. Las membranas dializantes están presentes
Aplicaciones
Hay dos métodos de diálisis: la hemodiálisis y la diálisis peritoneal.
En la diálisis peritoneal se infunde dentro de la cavidad abdominal un líquido que contiene una mezcla específica de glucosa y sales que arrastran las sustancias toxicas de los tejidos. Luego se extrae el líquido y se desecha.
La diálisis es una técnica común de laboratorio, y funciona con el mismo principio que diálisis médica. Típicamente una solución de varios tipos de moléculas es puesta en un bolso semipermeable de diálisis, como por ejemplo, en una membrana de la celulosa con poros, y el bolso es sellado. El bolso de diálisis sellado se coloca en un envase con una solución diferente, o agua pura. Las moléculas lo suficientemente pequeñas como para pasar a través de los poros (a menudo agua, sales y otras moléculas pequeñas) tienden a moverse hacia adentro o hacia afuera del bolso de diálisis en la dirección de la concentración más baja. Moléculas más grandes (a menudo proteínas, ADN) que tiene dimensiones significativamente mayores que el diámetro del poro son retenidas dentro del bolso de diálisis. Una razón común de usar esta técnica puede ser para quitar la sal de una solución de la proteína. La técnica no distinguirá efectivamente entre proteínas.
Soluciones Isotónicas
Un medio o solución isotónica es aquel en el cual la concentración de soluto es igual fuera y dentro de una célula, es decir,
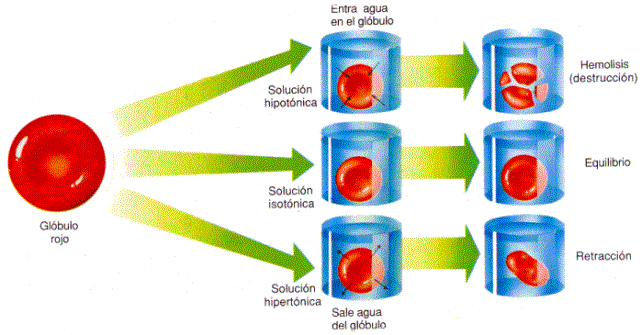
En hematología, se dice de las soluciones que tienen la misma concentración de sales que las células de la sangre son isotónicas. Por tanto, tienen la misma presión osmótica que la sangre y no producen la deformación de los glóbulos rojos.
Aplicaciones
En Medicina es muy común usar soluciones isotónicas en los casos de intervenciones quirúrgicas, quemaduras, diarreas, vómitos repetidos, etc., para corregir las alteraciones del balance hidroelectrolítico. La solución de NaCl al 0,9%, la de Dextrosa al 5%, tienen una molaridad cercana a la del plasma humano y por ello, son iso-osmóticas. También son isotónicas ya que no producen, al ser inyectadas por vía endovenosa, cambios notables en el volumen de los glóbulos rojos u otras células. En Medicina se usan, por lo general, soluciones para inyectar por vía endovenosa que están constituidas, en su mayor parte, por glucosa y NaCl. Como ambos generan partículas con un coeficiente reflexión, en las membranas celulares, de = 1, o muy cercano a él, se puede aceptar el uso, en la jerga médica, de isotónico como sinónimo de iso-osmótico. Sin embargo esto no siempre es válido y se debe estar muy alerta.
Ah mucha, pero mucha información, eso si es muy buena y eficaz, muy útil, buena fuente
ResponderBorrar